ぶどう膜炎の診療を続けていると、ある種の患者さんの増え方に気づきます。
リウマチや乾癬、強直性脊椎炎の治療中、あるいはがんの免疫療法を受けている最中に「目が赤い」「かすむ」「ゆがんで見える」という訴えで眼科を受診される方が、以前より確実に増えています。
投薬内容を確認すると、バイオ製剤や分子標的薬の名前を見つけます。
私自身は以前、九大の免疫学教室(九州大学生体防御医学研究所)で「サイトカイン」の基礎研究をしていた時期があります。
IL-6, TNF-α, IL-17A;こうした炎症性の分子を制御することで病気を治せるはずだという考え方は、研究者として皆ごく自然な発想でした。
自分たちが研究室で扱っていた分子が、実際の薬として次々と登場してくる:そういう時代になったのかと思いました。
📌 サイトカインとは
免疫細胞から分泌される小さなタンパク質で、細胞間の「連絡役」として働きます。
炎症を起こす・抑える・免疫細胞を呼び寄せるなど、体の免疫反応を調整する司令塔のような存在です。
IL-6・TNF-α・IL-17Aなどが代表例で、これらが過剰に働くことで関節リウマチや乾癬などの自己免疫疾患が起きます。
バイオ製剤によって、このサイトカインを狙い撃ちにします。
ところが実際に診療を続けると、そこには思いがけない現実がありました。
TNF-αを遮断したはずなのに眼に炎症が起きる。IL-17Aを抑えたのに炎症は起こったままになる。免疫のブレーキを外したら自分の眼を攻撃し始める!
こういった患者さんの目に起きていることは、単なる「副作用」という言葉では説明しきれないことがあります。
眼という臓器が持っている、特別な免疫のしくみが関わっているからです。
バイオ製剤や免疫治療薬が、そのしくみをどのように書き換えてしまうのか。
そして、感染症によるぶどう膜炎が「偶然起きる」のではなく「封じ込め機能の崩壊」として起きるのはなぜか。
この記事では、その背景にある考え方を整理します。

眼は「免疫の特区」である
眼という臓器は、免疫学の観点からは非常に特殊な場所です。
1940年代にサー・ピーター・メダワーが行った実験で、眼の中(前房内)に移植した組織が、他の場所に移植した場合よりも長く生き残ることが観察されました¹。
これが「眼免疫特権(ocular immune privilege)」という概念の出発点です。
眼が特別な理由は、視機能を守るためです。
眼の炎症は特殊で、その透明性を最大限に残したままで治癒することが大切です。
網膜は、一度傷ついてしまうと再生しません。
眼組織に瘢痕を残して治癒した場合、一生の視力に影響を及ぼします。
そのため眼は、炎症によって自分自身を傷つけないよう、特別な抑制システムを備えています。
血液網膜関門(blood-retinal barrier, BRB)という物理的なバリアが、血液中の免疫細胞や病原体が眼の中に入るのを防いでいます。
それだけでなく、眼の中の液体(房水・硝子体)には炎症を抑える物質が含まれており、たとえ免疫細胞が侵入してきても、その活動を減弱させるよう働きます²。
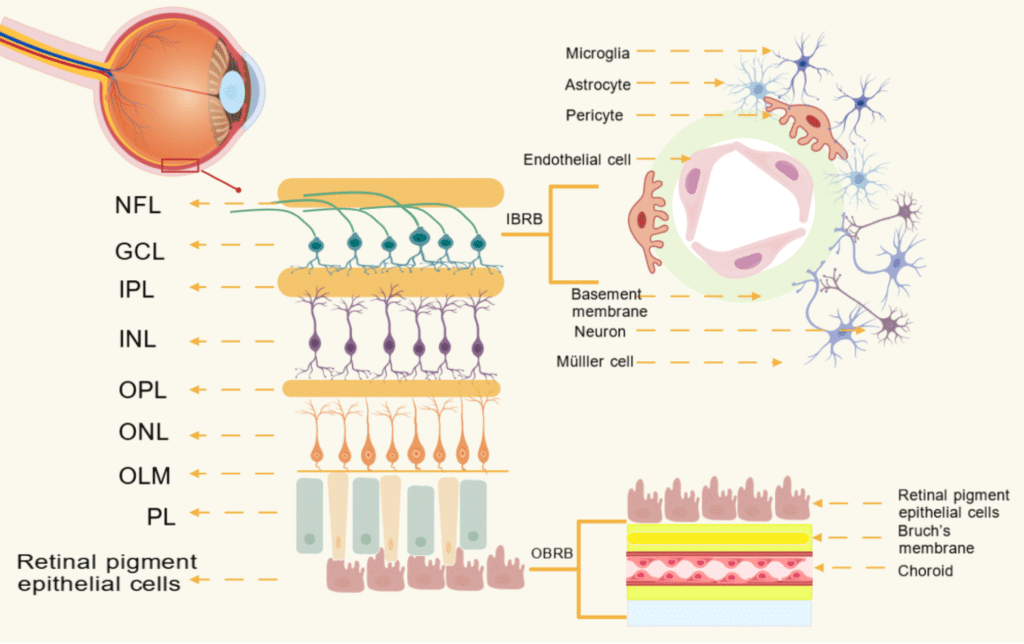
血液網膜関門は内側(iBRB)と外側(oBRB)の2層から構成されています。iBRBは網膜血管内皮細胞・周皮細胞・ミクログリア・アストロサイト・ミュラー細胞からなる神経血管ユニットで形成され、外側oBRBは網膜色素上皮細胞・ブルッフ膜・脈絡膜毛細血管で構成されています。これら2つのバリアが協調して網膜の恒常性を維持しており、どちらか一方が破綻することが糖尿病網膜症をはじめとする多くの網膜疾患の発症につながります。
Schematic diagram of the blood-retinal barrier (BRB) structure. The inner BRB (iBRB) comprises retinal vascular endothelial cells, pericytes, microglia, astrocytes, and Müller cells forming the neurovascular unit. The outer BRB (oBRB) consists of retinal pigment epithelial cells, Bruch’s membrane, and the choriocapillaris. Disruption of either barrier underlies the pathogenesis of diabetic retinopathy and other retinal diseases.
Li M et al. Front Endocrinol. 2025;16:1617797. Adapted under CC BY 4.0. https://www.frontiersin.org/journals/endocrinology/articles/10.3389/fendo.2025.1617797/full
また、眼の中に抗原が入ると、脾臓を介して「この抗原には過剰反応しない」という全身的なシグナルが生まれます。これを「前房関連免疫偏位(Anterior Chamber-Associated Immune Deviation, ACAID)」と呼びます³。
現代の免疫学では、眼免疫特権は単なる「隔離」ではなく、「能動的な免疫調節システム」として理解されています⁴。
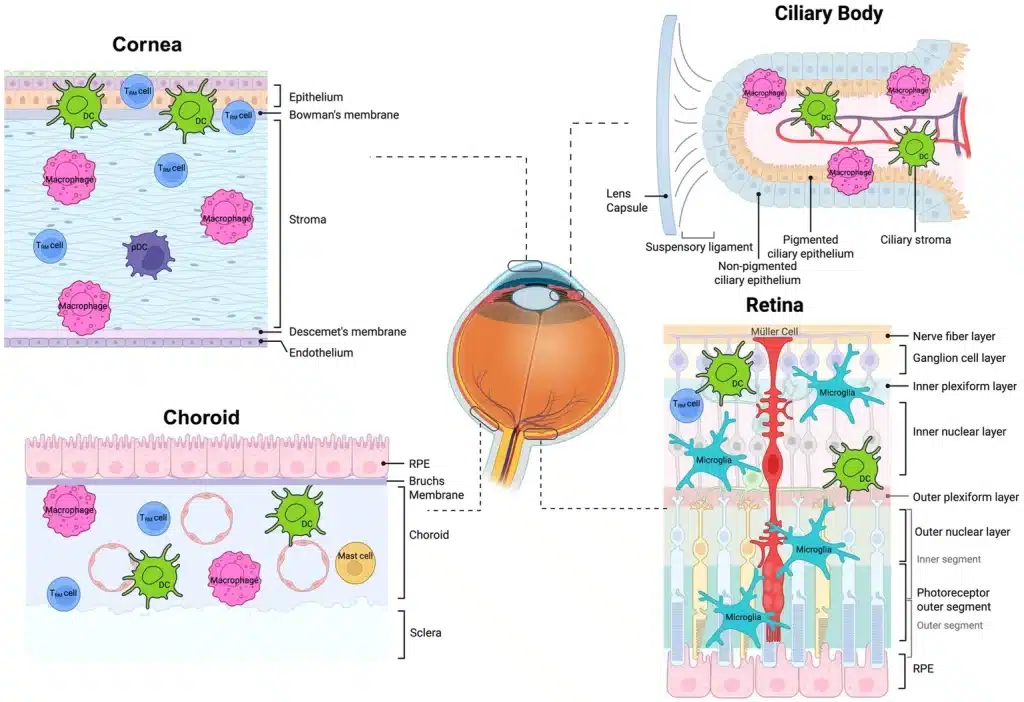
眼は免疫特権を持つ臓器ですが、角膜・毛様体・脈絡膜・網膜のそれぞれに組織常在免疫細胞(組織常在メモリーT細胞、樹状細胞、形質細胞様樹状細胞など)が存在し、恒常性の維持と炎症応答の調節を担っています。こうした常在免疫細胞のバランスが崩れることが、ぶどう膜炎の発症に関わると考えられています。
Figure showing tissue-resident immune populations present in healthy normal eyes across distinct ocular microenvironments, including tissue-resident memory T cells (T_RM), dendritic cells (DCs), and plasmacytoid dendritic cells (pDCs).
Han et al. Front Med. 2026;13:1717056. Adapted under CC BY 4.0. https://www.frontiersin.org/journals/medicine/articles/10.3389/fmed.2026.1717056/full
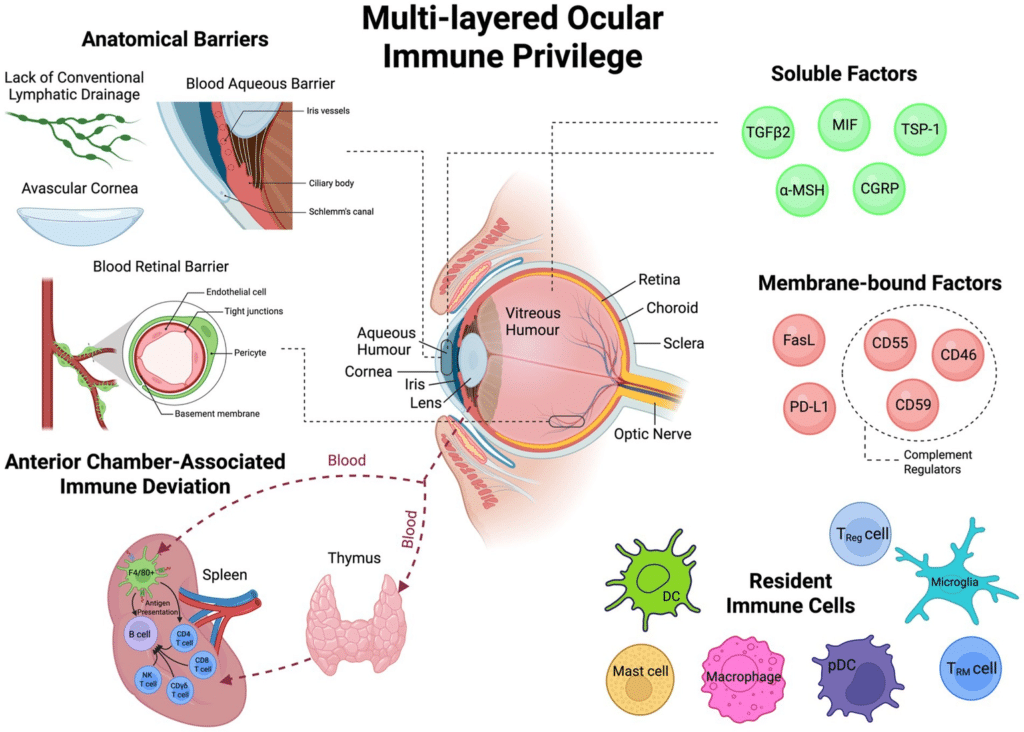
眼が「免疫の特区」として機能する背景には、複数の防御機構が重なり合っています。解剖学的バリア(無血管角膜・血液房水関門・血液網膜関門・リンパ管の欠如)、免疫抑制性の可溶性因子(TGFβ2・MIF・TSP-1・α-MSH・CGRPなど)、膜結合型因子(FasL・PD-L1・補体調節因子)、そして前房関連免疫偏向(ACAID)による全身性免疫寛容の誘導が組み合わさることで、眼内の炎症は厳密に制御されています。常在免疫細胞(樹状細胞・マクロファージ・ミクログリア・制御性T細胞など)もこの恒常性維持に重要な役割を担っています。
Schematic diagram illustrating the multi-layered mechanisms of ocular immune privilege, including anatomical barriers, soluble immunosuppressive factors, membrane-bound regulators, anterior chamber-associated immune deviation (ACAID), and resident immune cells.
Han et al. Front Med. 2026;13:1717056. Adapted under CC BY 4.0. https://www.frontiersin.org/journals/medicine/articles/10.3389/fmed.2026.1717056/full
バイオ製剤(生物学的製剤)とはどういう薬か
バイオ製剤(生物学的製剤)は、免疫反応に直接関わる特定の分子——サイトカインや細胞表面の受容体——を標的とした薬剤です。
リウマチ・乾癬・強直性脊椎炎・クローン病・がん治療など、幅広い疾患に使われています。

バイオ製剤の主なクラスを整理すると、以下のようになります。
抗TNF-α製剤(腫瘍壊死因子-α阻害剤)は最も歴史が長く、インフリキシマブ、アダリムマブ、エタネルセプトなどが代表です。
IL-17阻害剤(セクキヌマブ、イキセキズマブなど)は特に乾癬・強直性脊椎炎に使われます。
JAK阻害剤(ウパダシチニブ、トファシチニブなど)は複数のサイトカインシグナルを同時に遮断する経口薬です。
そして免疫チェックポイント阻害剤(ペムブロリズマブ、ニボルマブ、イピリムマブなど)は、がんの免疫療法として使われています。
これらの薬は、免疫系の「過剰な反応」を抑えることで全身疾患をコントロールします。しかしその一方で、眼が独自に維持していた免疫の均衡を乱すことがあります。
なぜバイオ製剤でぶどう膜炎が起きるのか
薬のクラスごとに、眼への影響のメカニズムが異なります。それぞれ順に見ていきます。
抗TNF-α製剤:逆説的な炎症が起きることがある
抗TNF製剤は、関節や皮膚の炎症を抑える一方で、眼の炎症を「かえって引き起こす」という逆説的な副作用が報告されています。
これは「パラドキシカル(逆説的)反応」と呼ばれます⁵。
特に注目されているのがエタネルセプトです。
同じ抗TNF製剤でも、モノクローナル抗体型(インフリキシマブ・アダリムマブ)と比べて、ぶどう膜炎の新規発症・再発リスクが高いことが複数の研究で示されています⁶。
強直性脊椎炎患者を対象にしたネットワークメタ解析では、エタネルセプトはゴリムマブやインフリキシマブと比べてぶどう膜炎リスクが2倍以上高いことが報告されています⁷。
なぜこの違いが生まれるのでしょうか。
TNF-αは炎症性サイトカインですが、同時に免疫細胞の一種(pDC)からの炎症シグナル(インターフェロン-α)産生を抑制する役割も持っています。
エタネルセプトは可溶型TNFのみを結合し、T細胞のアポトーシス誘導効果が弱いため、TNF遮断によってインターフェロン産生が逆に高まり、肉芽腫性炎症を誘発しやすいと考えられています。
モノクローナル抗体型はより強力にこのシフトを抑制するため、ぶどう膜炎リスクが相対的に低いとされています⁸。
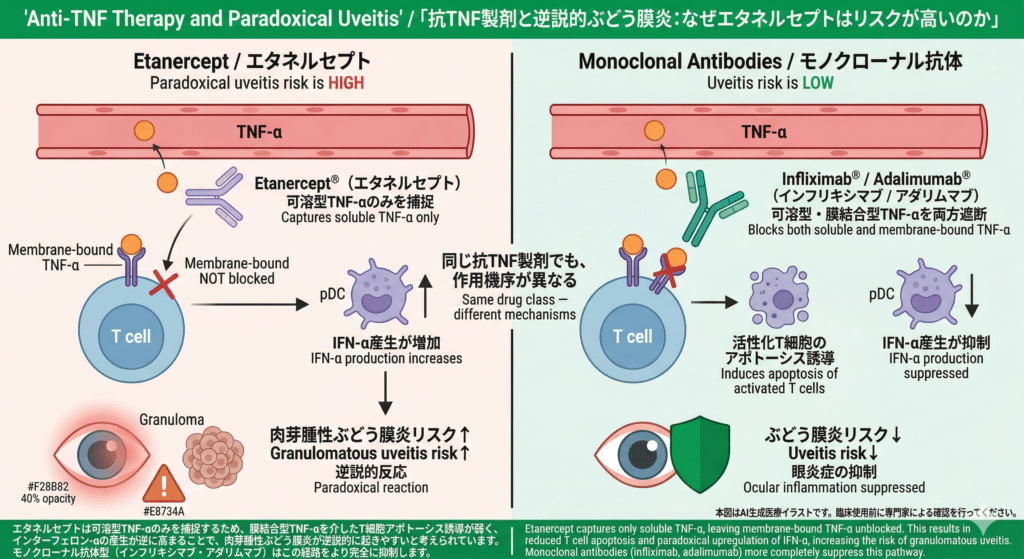
同じ抗TNF製剤でも、作用機序によって眼への影響は異なります。(左)エタネルセプトは可溶型TNF-αのみを捕捉し、膜結合型TNF-αを介したT細胞アポトーシス誘導が弱いため、形質細胞様樹状細胞(pDC)からのIFN-α産生が逆に高まり、肉芽腫性ぶどう膜炎が逆説的に起きやすいと考えられています。(右)インフリキシマブ・アダリムマブなどのモノクローナル抗体は可溶型・膜結合型TNF-αの両方を遮断し、この経路をより完全に抑制します。
Schematic diagram illustrating the differential mechanisms of etanercept versus anti-TNF monoclonal antibodies in paradoxical uveitis. Etanercept captures only soluble TNF-α, leaving membrane-bound TNF-α unblocked, resulting in reduced T cell apoptosis and paradoxical IFN-α upregulation that increases granulomatous uveitis risk. Monoclonal antibodies (infliximab, adalimumab) block both soluble and membrane-bound TNF-α, more completely suppressing this pathway.
AI-generated medical illustration / たける眼科, 2026.
IL-17阻害剤:バリアを守っていた物質を遮断してしまう
セクキヌマブやイキセキズマブなどのIL-17阻害剤は、乾癬や強直性脊椎炎に非常に効果的な薬剤ですが、ぶどう膜炎との関係は複雑です。
IL-17Aは炎症性のサイトカインである一方、眼のバリア機能(タイトジャンクション)を守る役割も持っています。
セクキヌマブが非感染性ぶどう膜炎の治療薬として期待され3つのランダム化比較試験(SHIELD・INSURE・ENDURE試験)が行われましたが、主要評価項目を達成することができませんでした⁹。
一方で、強直性脊椎炎患者に使われた場合にぶどう膜炎を「新たに引き起こす」あるいは「再発させる」という報告も存在します。
2024年の大規模ネットワークメタ解析によれば、IL-17A単独の阻害(セクキヌマブ・イキセキズマブ)はプラセボより眼に不利な可能性があり、IL-17AとIL-17Fを同時に阻害するビメキズマブは逆にぶどう膜炎リスクを有意に低下させることが示されています⁷。
IL-17AだけでなくIL-17Fも遮断することで、バリア保護を維持しながら病原的な炎症経路をより完全に抑えられるためと考えられています。
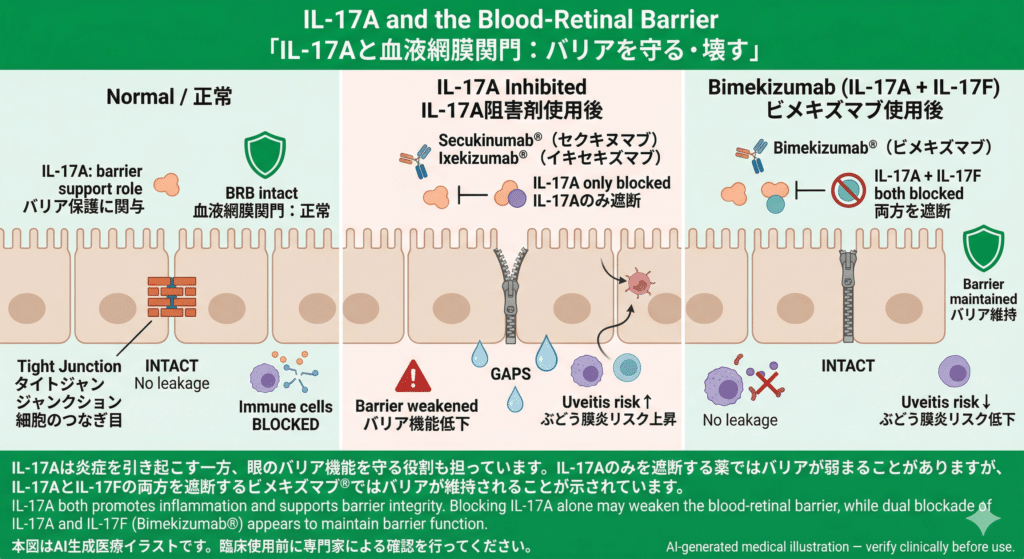
IL-17Aのみを遮断する製剤(セクキヌマブ・イキセキズマブ)ではバリア機能が低下しぶどう膜炎リスクが上昇する一方、IL-17AとIL-17Fの両方を遮断するビメキズマブではバリアが維持されリスクが低下することが示されています。
Schematic diagram illustrating the effect of IL-17 inhibitors on the blood-retinal barrier. Blocking IL-17A alone (secukinumab, ixekizumab) may weaken barrier function and increase uveitis risk, while dual blockade of IL-17A and IL-17F (bimekizumab) appears to maintain barrier integrity.
AI-generated medical illustration / たける眼科, 2026.
(余談)IL-17Aの遺伝子を持たないマウスで実験的ぶどう膜炎を起こそうとしたところ、抑制されると予想していた炎症があまり差がなかったという論文を発表したことがあります。当時は不思議に思っていましたが、今になって納得できました。
JAK阻害剤:ウイルスを「封じ込める力」が失われる
JAK阻害剤(JAK1/2/3阻害剤)は、インターロイキン-2・6・インターフェロンなど複数のサイトカインシグナルを広範に遮断します。
この「広範な遮断」は、眼の中でウイルスを抑え込んでいたインターフェロン依存的な防御を崩すことがあります。
免疫が正常な状態では滅多に起きないサイトメガロウイルス(cytomegalovirus, CMV)網膜炎や水痘帯状疱疹ウイルス(varicella-zoster virus, VZV)による壊死性網膜炎が、JAK阻害剤使用中に報告されています。
しかも、こうした感染性網膜炎は、通常見られるような硝子体混濁などの炎症所見をほとんど伴わないことがあります。
これは、ウイルスの増殖を許す機能不全と、炎症細胞を動員するシグナルが同時に遮断されることで、「静かに進行する壊死」という非常に危険な臨床像をとりうることを意味します¹⁰。
JAK阻害剤使用中に視覚症状が出た際には、感染性の病態を積極的に除外する必要があります。
免疫チェックポイント阻害剤:眼の「自己寛容」を解除してしまう
がん治療に使われるPD-1/PD-L1阻害剤(ペムブロリズマブ・ニボルマブなど)やCTLA-4阻害剤(イピリムマブ)は、免疫の「ブレーキ」を外すことでがん細胞への攻撃を強化します。
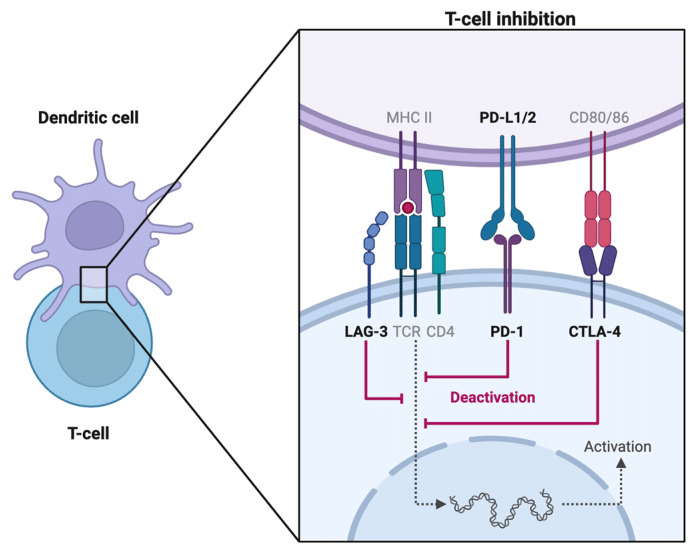
(左)通常、T細胞上のPD-1ががん細胞や抗原提示細胞のPD-L1と結合することでT細胞活性が抑制され、腫瘍が免疫から逃れます。同様にCTLA-4はCD28と競合してT細胞の活性化を初期段階で抑制します。(右)抗PD-1/PD-L1抗体・抗CTLA-4抗体はこの抑制シグナルを遮断し、T細胞の「ブレーキ」を解除することでがん細胞への攻撃を回復させます。
Schematic diagram illustrating the mechanisms of immune checkpoint inhibition. (Left) Under normal conditions, PD-1 on T cells binds to PD-L1 on cancer cells or antigen-presenting cells, suppressing T cell activity and allowing tumor immune evasion. CTLA-4 similarly dampens T cell activation at an earlier stage. (Right) Anti-PD-1/PD-L1 and anti-CTLA-4 antibodies block these inhibitory interactions, restoring T cell activity against cancer cells.
Zhang H et al. Diagnostics. 2024;14(3):336. Adapted under CC BY 4.0. https://pmc.ncbi.nlm.nih.gov/articles/PMC10855398/
しかしその「ブレーキを外す」という作用は、本来は健康な自己組織への攻撃を抑えるためにも使われていたものです。
眼の場合、PD-1/PD-L1経路は網膜やぶどう膜のメラノサイト(色素細胞)に対する自己免疫反応を抑制する役割を担っています。
この経路を遮断すると、眼の中のメラノサイトへの免疫攻撃が始まり、原田病(Vogt-Koyanagi-Harada disease, VKH)に酷似した両眼性の肉芽腫性汎ぶどう膜炎が発症することがあります¹¹。
2024年の系統的レビューでは、52例のVKH様ぶどう膜炎が報告され、その69%が悪性黒色腫の患者さんであったことが示されています¹²。
悪性黒色腫はもともとメラノサイトの癌化であるため、腫瘍と眼のメラノサイトが「同じ標的」になりやすいという関係があります。
また、イピリムマブ(CTLA-4阻害剤)のぶどう膜炎発症リスク(ハザード比)は30.5と非常に高く、PD-1阻害剤の単剤(ハザード比:1.98)と比べて際立っています¹³。
興味深いことに、こうした眼の免疫反応は全身のがんに対する強い免疫応答のマーカーになる可能性も示唆されており、腫瘍予後との相関を検討した研究も出始めています。
感染症によるぶどう膜炎は「偶然起きた」のではない
ここからが、この記事の核心です。
バイオ製剤や免疫治療薬を使っている患者さんに、結核・梅毒・ヘルペスウイルス・CMVなどの感染症が起こることがあります。
これを「運が悪かった」「たまたまもらった感染症」として捉えるのは、正確ではありません。
眼は本来、病原体を「封じ込める力」を持っている。薬がその力を壊したとき、封じ込められていたものが動き出す——そういう構造で起きていることです。
ヘルペスウイルス・CMV:潜伏していたウイルスが再活性化する
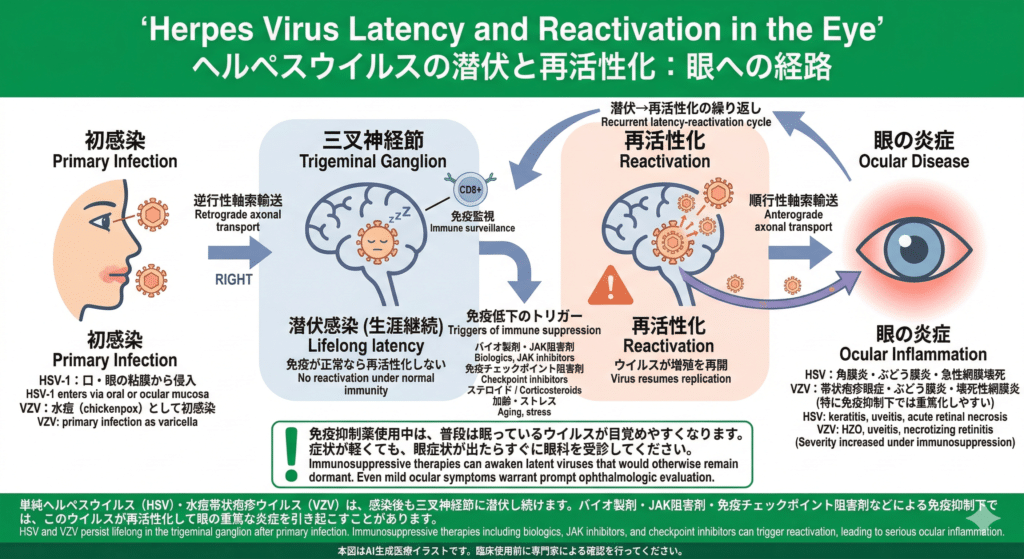
単純ヘルペスウイルス(HSV)・水痘帯状疱疹ウイルス(VZV)は、初感染後も三叉神経節に生涯潜伏し続けます。免疫が正常であれば再活性化しませんが、バイオ製剤・JAK阻害剤・免疫チェックポイント阻害剤・ステロイドなどによる免疫抑制下では、潜伏していたウイルスが再活性化し、順行性軸索輸送(神経の経路をたどって眼へ移動すること)によって眼に到達して重篤な炎症を引き起こします。HSVでは角膜炎・ぶどう膜炎・急性網膜壊死、VZVでは帯状疱疹眼症・ぶどう膜炎・壊死性網膜炎が起こることがあります。
Schematic diagram illustrating the latency-reactivation cycle of HSV and VZV in the eye. After primary infection, both viruses establish lifelong latency in the trigeminal ganglion. Immunosuppressive therapies including biologics, JAK inhibitors, and checkpoint inhibitors can trigger reactivation, with anterograde axonal transport leading to serious ocular inflammation including keratitis, uveitis, and retinal necrosis.
AI-generated medical illustration / たける眼科, 2026.
単純ヘルペスウイルス(herpes simplex virus, HSV)や水痘帯状疱疹ウイルス(VZV)は、感覚神経節に潜んでいます。
免疫が正常であれば、ウイルスは潜伏したままです。
しかしステロイドや免疫抑制薬、特にJAK阻害剤によってインターフェロン系の防御が弱まると、ウイルスが再活性化し、角膜炎・ぶどう膜炎・急性網膜壊死などを引き起こします¹⁰。

CMVは角膜内皮や眼内組織に潜伏することができます。
JAK阻害剤やその他の強力な免疫抑制剤の使用中に、局所での免疫監視が失われるとCMVが増殖し始めます。
眼のインターフェロン依存的防御が「内側から崩れる」という点が、このタイプの感染の特徴です。
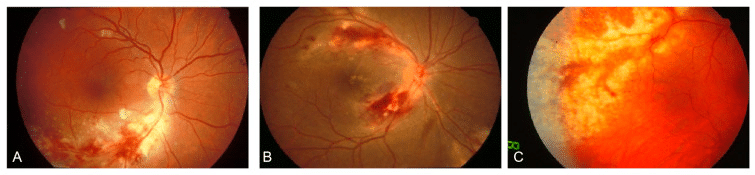
免疫が低下した状態でCMVが眼内で再活性化すると、網膜炎を引き起こします。(A) 早期:視神経乳頭周囲の黄白色壊死病巣と網膜内出血。(B) 進行期・出血型:後極部を中心とした全層性網膜壊死と出血、活動辺縁の衛星病巣——いわゆる「ピザパイ」様所見。(C) 顆粒型:周辺部から後極に向かって拡大する融合性白色壊死病巣。
Fundus photographs of cytomegalovirus (CMV) retinitis showing three distinct presentations. (A) Early-stage retinitis with yellowish-white necrotic lesions and intraretinal hemorrhage around the optic disc. (B) Advanced hemorrhagic variant with full-thickness retinal necrosis and “pizza pie” appearance. (C) Peripheral granular variant with confluent white necrotic lesions spreading toward the posterior pole.
Zhang J et al. Viruses. 2024;16(9):1427. Adapted under CC BY 4.0. https://pmc.ncbi.nlm.nih.gov/articles/PMC11437412/
結核:目立たない共存が、突然崩れる
眼内の潜伏結核は比較的まれですが、体内のどこかに潜んでいた結核菌が抗TNF製剤によって再活性化し、眼に至ることがあります。
通常の眼内結核は脈絡膜結節などの比較的わかりやすい像を呈しますが、抗TNF製剤下で起きた場合は、蛇行状脈絡膜炎(serpiginous-like choroiditis)のような広範な組織壊死を伴う非定型の像をとることがあります。
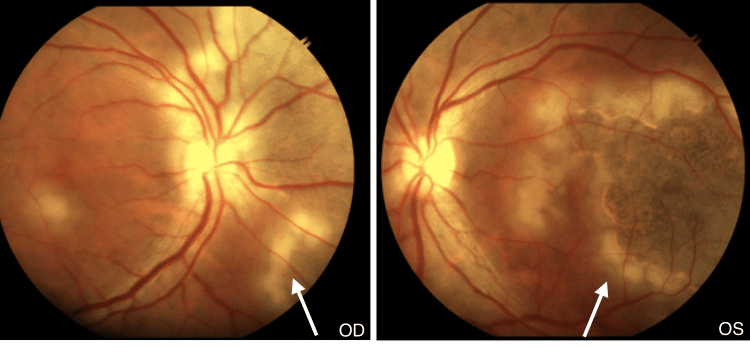
結核菌感染に伴うぶどう膜炎は、脈絡膜結節などの典型像だけでなく、蛇行状脈絡膜炎様の広範な組織壊死を呈することがあります。右眼(OD)・左眼(OS)ともに、矢印で示した領域に灰黄色の網膜下浸潤が蛇行状に拡大している様子が確認できます。
Fundus photographs of both eyes showing tubercular serpiginous-like choroiditis. Grey-yellowish subretinal infiltrates spreading in a serpiginous pattern are visible in the right eye (OD) and left eye (OS), with active scalloped edges at the advancing margin (arrows).
Magdum R et al. Cureus. 2024;16(3):e57093. Adapted under CC BY 4.0. https://pmc.ncbi.nlm.nih.gov/articles/PMC11055604/
これは、結核菌そのものの増殖だけでなく、TNF-αによって維持されていた肉芽腫の封じ込め構造が崩壊し、「無秩序な過敏反応」が起きた結果と考えられています¹⁴。
抗TNF製剤の開始前にインターフェロン-γ遊離試験(QuantiFERON検査)などで潜在性結核のスクリーニングが必要とされているのは、この理由からです。
梅毒:沈静化していたものが、動き出す
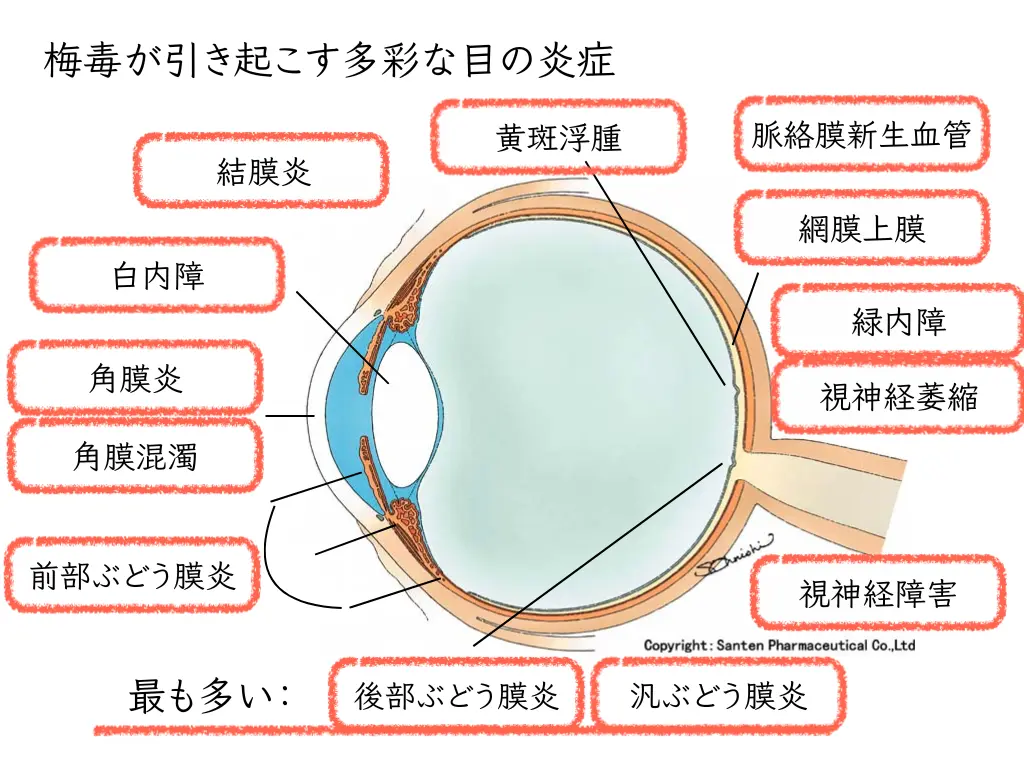
梅毒は近年、国内でも増加傾向にある感染症です。免疫機能が低下した状態では、通常よりも重篤な眼梅毒(ocular syphilis)を発症する可能性があります。

ぶどう膜炎、視神経炎、脈絡網膜炎など多彩な形で眼に現れます。
バイオ製剤使用中や免疫チェックポイント阻害剤使用中の患者さんで、説明のつかないぶどう膜炎を見たときは、梅毒血清反応を含めた感染スクリーニングが重要です¹⁰。
「眼の免疫封じ込め機能」という視点で考える
ここまで見てきたことを整理すると、次のように言えます。
眼の中には、微生物や炎症誘発物質を「封じ込める」能力が備わっています。
血液網膜関門・抑制性サイトカイン・インターフェロン系防御・ACAID——これらが組み合わさって、眼は炎症から守られています。
バイオ製剤や免疫治療薬は、全身疾患の治療のために必要な薬です。
しかしそれらが眼の免疫バランスに作用するとき、どの防御機構が影響を受けるかによって、異なるタイプのぶどう膜炎が引き起こされます。
| 薬剤クラス | 眼への主な影響 | 起こりやすい病態 |
|---|---|---|
| 抗TNF製剤(特にエタネルセプト) | インターフェロン産生の逆説的増加 | 肉芽腫性ぶどう膜炎、逆説的炎症 |
| IL-17A阻害剤 | バリア保護因子の減弱 | 新規・再発前部ぶどう膜炎 |
| JAK阻害剤 | ウイルス防御(IFN系)の消失 | CMV・VZV網膜炎(非典型) |
| 免疫チェックポイント阻害剤 | 自己寛容チェックポイントの解除 | VKH様汎ぶどう膜炎 |
| 感染症(TB・梅毒・ヘルペス等) | 封じ込め機構の崩壊による再活性化 | 肉芽腫性・壊死性ぶどう膜炎 |
感染症によるぶどう膜炎は、この表の「感染症」欄と、それ以外の薬剤行が交差するところで起きます。薬が免疫の封じ込めを弱め、潜伏していた病原体が動き出す——という順序です。
こんな症状が出たときは
バイオ製剤・免疫チェックポイント阻害剤を使っている方で、以下のような症状が出た場合は眼科への受診が勧められます。
目の充血が続く、目が痛い、かすんで見える、ゆがんで見える、光がまぶしい、視力の変化に気づく——これらはぶどう膜炎の一般的なサインです。
ただし、JAK阻害剤やステロイド使用中は「炎症を示すサインが出にくい」ことがあるため、症状が軽くても注意が必要です。
「目が少し変」という程度の訴えでも、放置していると取り返しのつかない視力低下につながることがあります。
薬剤名と投与量を把握している主治医(リウマチ科・腫瘍内科・皮膚科など)と連携しながら、眼科での精密検査を受けることが大切です。

今後どうなっていくのか
バイオ製剤と眼炎症の研究は、現在も急速に進んでいます。
IL-17AとIL-17Fを同時に阻害するビメキズマブは、従来のIL-17A単独阻害と比べてぶどう膜炎リスクを下げながら関節・皮膚症状を強力に改善できることが示されつつあります⁷。
免疫チェックポイント阻害剤関連の眼副作用については、発症のタイミング・重症度・治療法の最適化に関するデータが集まりつつあります¹²¹³。
JAK阻害剤については、どの経路の遮断が眼の感染リスクに最も関与しているかが検討されています。
抗HIV療法や全身の免疫抑制中止後にも、封じ込めていた病原体に対する免疫が急に立ち上がることで「immune recovery uveitis」と呼ばれる炎症が起こることが知られており、同じ「封じ込め機構の揺り戻し」という文脈で理解できます¹⁴。
眼科医としての立場から、
このようなバイオ薬剤を使っている患者さんの眼を定期的に確認することの重要性は、今後さらに高まることと考えています。
バイオ製剤を使いながらも視力を守るためには、眼科と主治医との情報共有が欠かせません。
本記事に登場する主な薬剤
抗TNF-α製剤(TNF阻害薬)
| 一般名 | 商品名(日本) | English | 投与経路 |
|---|---|---|---|
| インフリキシマブ | レミケード® | infliximab / Remicade® | 点滴静注 |
| アダリムマブ | ヒュミラ® | adalimumab / Humira® | 皮下注射 |
| エタネルセプト | エンブレル® | etanercept / Enbrel® | 皮下注射 |
| ゴリムマブ | シンポニー® | golimumab / Simponi® | 皮下注射 |
IL-17阻害剤
| 一般名 | 商品名(日本) | English | 投与経路 |
|---|---|---|---|
| セクキヌマブ | コセンティクス® | secukinumab / Cosentyx® | 皮下注射 |
| イキセキズマブ | トルツ® | ixekizumab / Taltz® | 皮下注射 |
| ビメキズマブ | ビムゼルクス® | bimekizumab / Bimzelx® | 皮下注射 |
JAK阻害剤
| 一般名 | 商品名(日本) | English | 投与経路 |
|---|---|---|---|
| ウパダシチニブ | リンヴォック® | upadacitinib / Rinvoq® | 経口 |
| トファシチニブ | ゼルヤンツ® | tofacitinib / Xeljanz® | 経口 |
免疫チェックポイント阻害剤
| 一般名 | 商品名(日本) | English | 投与経路 |
|---|---|---|---|
| ペムブロリズマブ | キイトルーダ® | pembrolizumab / Keytruda® | 点滴静注 |
| ニボルマブ | オプジーボ® | nivolumab / Opdivo® | 点滴静注 |
| イピリムマブ | ヤーボイ® | ipilimumab / Yervoy® | 点滴静注 |
※本記事中の薬剤名は、一般名・代表的な国内商品名・英語表記を併記しています。実際の処方内容・用法用量はお薬手帳や添付文書、または主治医にご確認ください。眼への影響については眼科専門医にご相談ください。
参考文献
- Medawar PB. Immunity to homologous grafted skin; the fate of skin homografts transplanted to the brain, to subcutaneous tissue, and to the anterior chamber of the eye. Br J Exp Pathol. 1948;29(1):58-69. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2073079/
- Streilein JW. Ocular immune privilege: therapeutic opportunities from an experiment of nature. Nat Rev Immunol. 2003;3(11):879-889. https://pubmed.ncbi.nlm.nih.gov/14668804/
- Taylor AW. Ocular immune privilege. Eye (Lond). 2009;23(10):1885-1889. https://doi.org/10.1038/eye.2008.382
- Redefining our vision: an updated guide to the ocular immune system. Nat Rev Immunol. 2024. https://www.nature.com/articles/s41577-024-01064-y
- Nicolela Susanna F, Pavesio C. A review of ocular adverse events of biological anti-TNF drugs. J Ophthalmic Inflamm Infect. 2020;10(1):11. https://link.springer.com/article/10.1186/s12348-020-00202-6
- Fabiani C, Vitale A, Lopalco G, et al. Different roles of TNF inhibitors in acute anterior uveitis associated with ankylosing spondylitis: state of the art. Clin Rheumatol. 2016;35(11):2631-2638. https://pubmed.ncbi.nlm.nih.gov/27686662/
- Zhao X, He X, et al. Risk of new-onset and recurrent uveitis with different biologics for ankylosing spondylitis: a network meta-analysis. Front Immunol. 2025. https://pmc.ncbi.nlm.nih.gov/articles/PMC12226306/
- Baughman RP, Lower EE, Bradley DA, Raymond LA, Kaufman A. Etanercept for refractory ocular sarcoidosis: results of a double-blind randomized trial. Chest. 2005;128(2):1062-1047. https://journal.chestnet.org/article/S0012-3692(15)50471-6/
- Dick AD, Tugal-Tutkun I, Foster S, et al. Secukinumab in the treatment of noninfectious uveitis: results of three randomized, controlled clinical trials. Ophthalmology. 2013;120(4):777-787. https://pubmed.ncbi.nlm.nih.gov/23290985/
- Teabagy S, Wood E, Bilsbury E, et al. Ocular immunosuppressive microenvironment and novel drug delivery for control of uveitis. Adv Drug Deliv Rev. 2023;198:114869. https://pubmed.ncbi.nlm.nih.gov/37172782/
- Sun MM, Levinson RD, Filipowicz A, et al. Uveitis in patients treated with CTLA-4 and PD-1 checkpoint blockade inhibition. Ocul Immunol Inflamm. 2020;28(2):217-227. https://pmc.ncbi.nlm.nih.gov/articles/PMC6832811/
- Zhang H, Houadj L, Wu KY, Tran SD. Immune checkpoint inhibitor-associated Vogt-Koyanagi-Harada-like syndrome: a descriptive systematic review. J Ophthal Inflamm Infect. 2025. https://link.springer.com/article/10.1186/s12348-025-00484-8
- Kuo HT, Chen CY, Hsu AY, et al. Association between immune checkpoint inhibitor medication and uveitis: a population-based cohort study utilizing TriNetX database. Front Immunol. 2024;14:1302293. https://pubmed.ncbi.nlm.nih.gov/38264654/
- Alves NR, Barão C, Mota C, Costa L, Pinto Proença R. Immune recovery uveitis: a focus review. Graefes Arch Clin Exp Ophthalmol. 2024;262(8):2703-2712. https://pubmed.ncbi.nlm.nih.gov/38381160/
![たける眼科 | 福岡市早良区 高取商店街[西新駅/藤崎駅]](https://takeru-eye.com/wp-content/uploads/2022/10/takeru_logo_for-WP-header.png)