皮膚がん「悪性黒色腫」に対しての分子標的薬
・ダブラフェニブ(タフィンラー®)
・トラメチニブ(メキニスト®)は、
ぶどう膜炎の副作用もあります。
目がかすむ、
ゆがんで見える
見えづらい
視力低下
目の充血
などの症状が出て、眼科を受診されることがあります。
新しい抗がん剤「分子標的薬」がひきおこすぶどう膜炎(目の副作用)
分子標的薬とは
免疫学の研究が進んできて、がんを進行させてしまう遺伝子やたんぱく質を特定できる時代になってきました。
ある遺伝子の変異があることで、がんが進行していることを知ることもできます。
がん細胞の遺伝子・たんぱく質に作用する薬を「分子標的薬」と呼びます。
異常な細胞増殖が起こることで、癌が進行します。
(=がん細胞が増えるスピードが速い)
化学療法で用いられる抗がん剤は、増殖の速い正常な細胞までも痛めてしまいます。
そのため、
・脱毛
・吐き気
・白血球減少
などの、重い副作用が出ていました。
細胞増殖に関わる分子をターゲットとすることで、以上のような副作用を減らすことができます1。
悪性黒色腫(メラノーマ)とは/新しい治療
悪性黒色腫(メラノーマ)は皮膚がんの一種で、
メラニン色素を作り出す細胞「メラノサイト」が、癌化してしまいます。
遺伝子は、体の中での特定の分子・たんぱく質を規定します。
そのうち、がん細胞増殖に関わる分子を特定することができてきました。
がん細胞の増殖を速くしてしまう「遺伝子の変異」も、わかってきました。
今では遺伝子の検査もおこなうことができます。
ある特定の遺伝子変異を確認できた方に、使うことができる薬ができました2,3。
「分子標的薬」と呼ばれています。
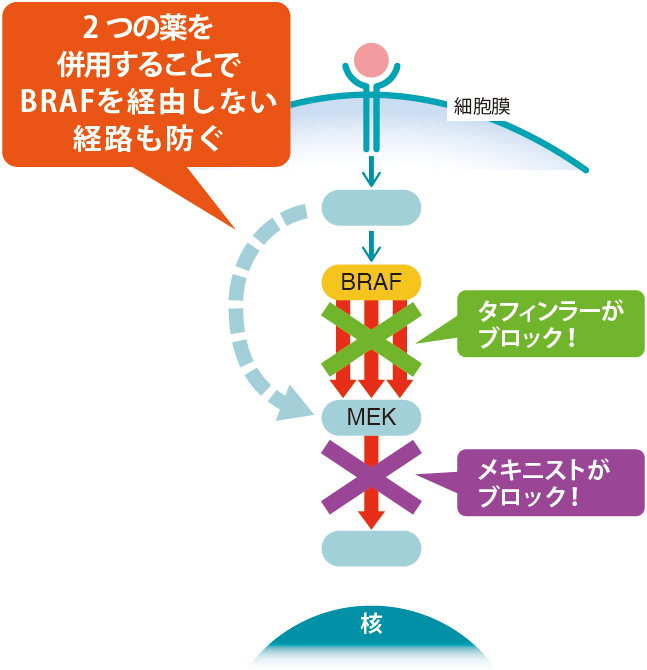
・ダブラフェニブ(タフィンラー®):BRAF阻害剤
・トラメチニブ(メキニスト®):MEK阻害剤
https://www.product.gan-kisho.novartis.co.jp/tafinlar-mekinist-info
パリに拠点を置くグスタフ・ルッシーがん研究所(Institut Gustave Roussy)の皮膚科科長のカロリーヌ・ロベール(Caroline Robert)医学博士は、次のように述べています。「『タフィンラー』『メキニスト』併用を一次治療とすることで、約5分の1の患者さんで5年間病状がコントロールされ、約3分の1が5年後も生存していたことが、今回の解析で明らかになりました。これまで転移性の悪性黒色腫の患者さんは予後不良とされていましたが、現在では希望を持てる要素も増えてきています。今回の解析は臨床意義が高く、患者さんの生存に好影響をもたらすでしょう。これらの結果は、分子標的療法が長期的な生存と持続的な転帰の改善をもたらしうることを示しています」
ノバルティス社HPより
・ダブラフェニブ(タフィンラー®)dabrafenib (Tafinlar)
・トラメチニブ(メキニスト®)trametinib (Mekinist)
ノバルティスファーマ:
https://www.product.gan-kisho.novartis.co.jp/tafinlar-mekinist-info
* 分子標的薬使用の組み合わせ(併用療法)は、下記もあります。
・エンコラフェニブ(ビラフトビ®)encorafenib (Braftovi)
・ビニメチニブ(メクトビ®)binimetinib (Mektovi)
小野薬品工業:
https://www.ono-oncology.jp/medical/products/mektovi/action
・ベムラフェニブ(ゼルボラフ®)vemurafenib (Zelboraf)
・コビメチニブ(コテリック®)cobimetinib (Cotellic)
Patient Access Scheme, “PAS”の評価から、
費用対効果評価が基準に満たされず「非推奨」とされている状態。
https://www.cotellic.com
目の「免疫学的特権」:炎症から眼球を守るしくみ
眼球は閉じられた臓器であることが、他の多くの臓器との違いです。
外からの炎症に対して免疫反応を引き起こし、眼球を守るはたらきがあります:
「免疫学的に特別な部位 “immune privileged site”」
目に入ってきた異物「抗原」に感作された細胞は、リンパ節から脾臓に運ばれて炎症を抑える細胞集団を作ります。
その細胞集団は目に戻ってきて、特定の抗原に対しての防御反応がはたらくことがわかっています4:
ACAID(Anterior Chamber-associated Immune Deviation; 前房関連免疫偏位)
血液網膜関門が正常に保たれていることが不可欠です。
血液網膜関門とは
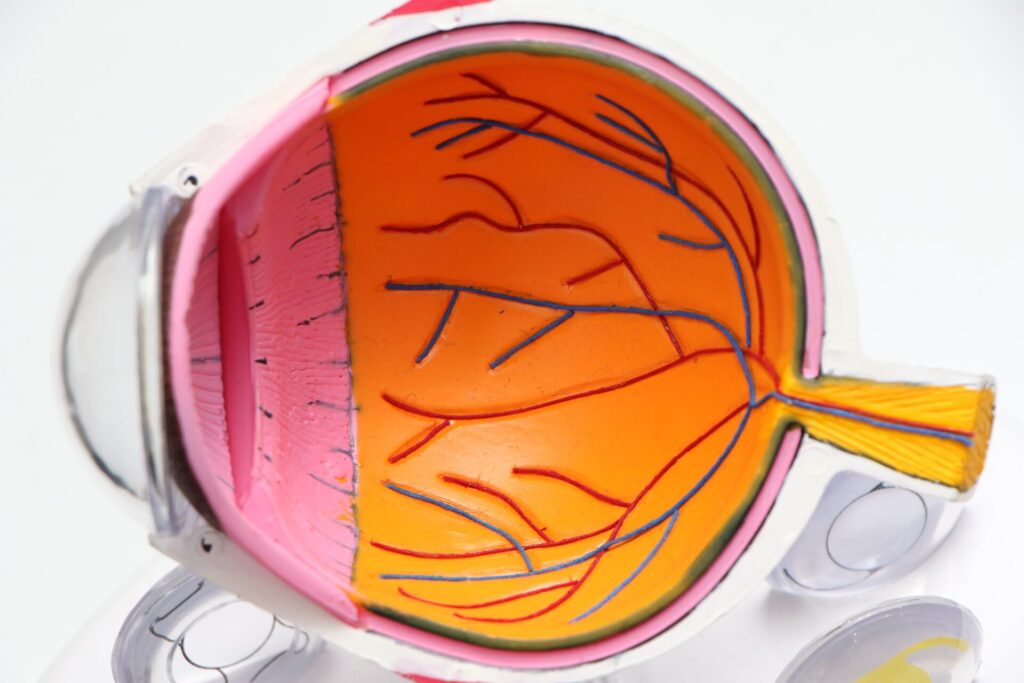
眼底写真を撮ると、きれいに網膜血管がみえます。
網膜はオレンジ色にみえるのは、奥側にある血管が豊富な組織「脈絡膜」の色が透けているからです。
血管の中を通る血液が漏れ出さないようにするバリアがあって、網膜の働きが正常に保たれています。
このことを、血液網膜関門(blood-retinal barrier)と名づけられています。
目の炎症「ぶどう膜炎」が起こっているときは、このバリアが破綻していることが知られています5。
糖尿病網膜症の発症・進行も、血液網膜関門の破綻が原因となります6。
分子標的薬「タフィンラー」「メキニスト」使用中のぶどう膜炎発症
「タフィンラー®」dabrafenib「メキニスト®」trametinibは、細胞増殖に関わる分子(MAPキナーゼ)に作用します。
血管の内側の細胞「血管内皮細胞」の増殖にも作用し、その働きを傷害させてしまうことも知られています。
血液網膜関門が障害されることにより、目の「免疫学的特権」を破綻させてしまう:
そして、炎症反応「ぶどう膜炎」を引き起こすことと考えられています7-10。
・網膜静脈閉塞症(Branch retinal vein occlusion, BRVO)
・中心性漿液性脈絡網膜症(Central serous chorioretinopathy, CSC)
も、この分子標的薬の副作用として重要です11, 12。
ぶどう膜炎・網膜疾患の初期症状
・目がかすむ
・目の充血
・いつもよりみえづらい
・視野に変化がある
・ものがゆがんでみえる 等
何か症状があれば、眼科受診をされてください。

参考文献
- Sullivan, R., LoRusso, P., Boerner, S., Dummer, R., 2015. Achievements and Challenges of Molecular Targeted Therapy in Melanoma. American Society of Clinical Oncology Educational Book 177–186. https://doi.org/10.14694/EdBook_AM.2015.35.177
- Menzies, A.M., Long, G.V., Murali, R., 2012. Dabrafenib and its potential for the treatment of metastatic melanoma. Drug Des Devel Ther 6, 391–405. https://doi.org/10.2147/DDDT.S38998
- Patel, H., Yacoub, N., Mishra, R., White, A., Yuan, L., Alanazi, S., Garrett, J.T., 2020. Current Advances in the Treatment of BRAF-Mutant Melanoma. Cancers 12, 482. https://doi.org/10.3390/cancers12020482
- Taylor, A.W., 2009. Ocular immune privilege. Eye 23, 1885–1889. https://doi.org/10.1038/eye.2008.382
- de Smet, M.D., Taylor, S.R.J., Bodaghi, B., Miserocchi, E., Murray, P.I., Pleyer, U., Zierhut, M., Barisani-Asenbauer, T., LeHoang, P., Lightman, S., 2011. Understanding uveitis: the impact of research on visual outcomes. Prog Retin Eye Res 30, 452–470. https://doi.org/10.1016/j.preteyeres.2011.06.005
- Kinuthia, U.M., Wolf, A., Langmann, T., 2020. Microglia and Inflammatory Responses in Diabetic Retinopathy. Front Immunol 11, 564077. https://doi.org/10.3389/fimmu.2020.564077
- Joshi, L., Karydis, A., Gemenetzi, M., Shao, E.H., Taylor, S.R.J., 2013. Uveitis as a Result of MAP Kinase Pathway Inhibition. Case Rep Ophthalmol 4, 279–282. https://doi.org/10.1159/000357060
- Rueda-Rueda, T., Sánchez-Vicente, J.L., Moruno-Rodríguez, A., Molina-Socola, F.E., Martínez-Borrego, A.C., López-Herrero, F., 2018. Uveitis and serous retinal detachment secondary to systemic dabrafenib and trametinib. Arch Soc Esp Oftalmol (Engl Ed) 93, 458–462. https://doi.org/10.1016/j.oftal.2018.01.008
- Draganova, D., Kerger, J., Caspers, L., Willermain, F., 2015. Severe bilateral panuveitis during melanoma treatment by Dabrafenib and Trametinib. J Ophthal Inflamm Infect 5, 17. https://doi.org/10.1186/s12348-015-0049-9
- Sarny, S., Neumayer, M., Kofler, J., El-Shabrawi, Y., 2017. Ocular toxicity due to Trametinib and Dabrafenib. BMC Ophthalmology 17, 146. https://doi.org/10.1186/s12886-017-0541-0
- van der Noll, R., Leijen, S., Neuteboom, G.H.G., Beijnen, J.H., Schellens, J.H.M., 2013. Effect of inhibition of the FGFR-MAPK signaling pathway on the development of ocular toxicities. Cancer Treat Rev 39, 664–672. https://doi.org/10.1016/j.ctrv.2013.01.003
- Niro, A., Strippoli, S., Alessio, G., Sborgia, L., Recchimurzo, N., Guida, M., 2015. Ocular Toxicity in Metastatic Melanoma Patients Treated With Mitogen-Activated Protein Kinase Kinase Inhibitors: A Case Series. American Journal of Ophthalmology 160, 959-967.e1. https://doi.org/10.1016/j.ajo.2015.07.035
![たける眼科 | 福岡市早良区 高取商店街[西新駅/藤崎駅]](https://takeru-eye.com/wp-content/uploads/2022/10/takeru_logo_for-WP-header.png)