オゼンピック・ビクトーザ・トルリシティ・バイエッタ・リキスミア・ビデュリオンなど、
GLP-1受容体作動薬が、糖尿病治療薬として広く使われるようになりました。
そしてマンジャロは、これらの薬剤とは異なり、GLP-1受容体とGIP受容体の両方に作用する新しいタイプの薬剤(デュアル作動薬)として注目を集めています。
特に、その強力な体重減少効果から「痩せ薬」として大きな関心を集めています。
日本糖尿病学会:インスリン製剤、GLP-1受容体作動薬 一覧表
https://www.jds.or.jp/uploads/files/education/insulin_glp-1_list_2024.pdf
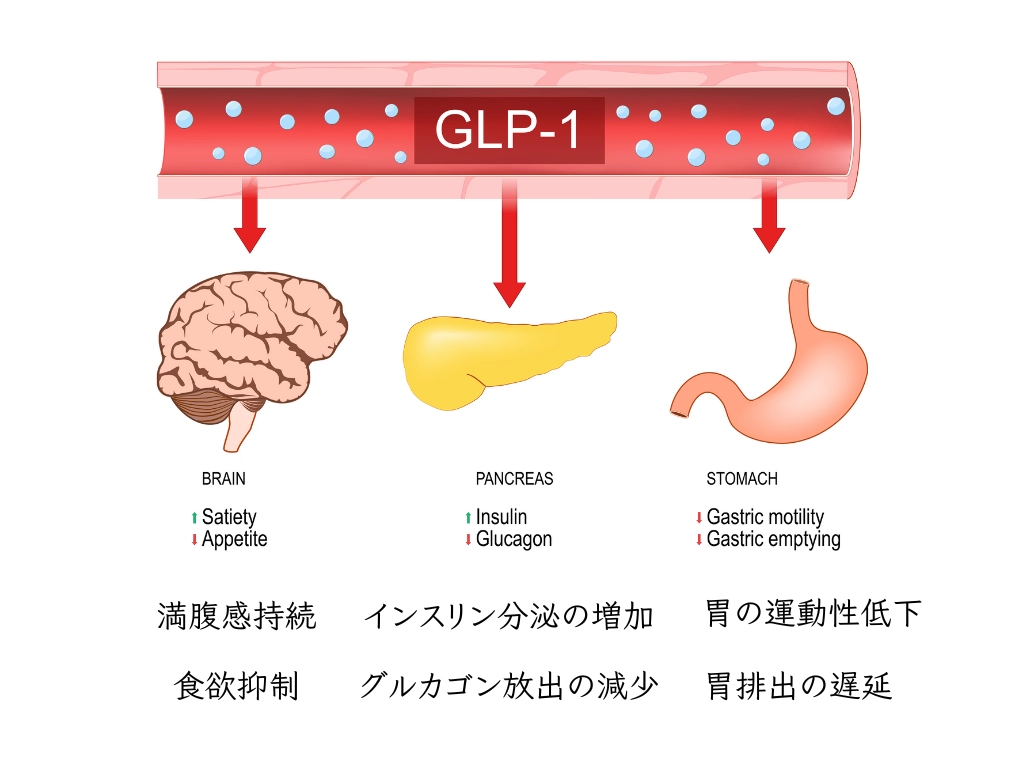
GLP-1は、膵臓から分泌されるインスリンの分泌を促すホルモンです。通常、食事をするとGLP-1が増加し、血糖値を下げる働きをします。
しかし、糖尿病患者さんではGLP-1の分泌が不足しているため、血糖値が上昇しやすくなります。
GLP-1受容体作動薬は、このGLP-1の働きを増強させる働きがあります。
一方で、急激に血糖を下げると短期的に糖尿病網膜症が悪化してしまうこともよく知られています。


GLP-1受容体作動薬と心血管に関しては、多くの臨床研究結果があります。
心血管に比べてとても細いのが、網膜の血管です。
網膜の血管は体内で唯一直視できる血管です。
そのため、眼底所見(網膜の血管)は心血管系の参考になることが知られています。

急激に血糖値を下げて、目の状態はどうなるか?
2023年最新のメタ解析1では、GLP-1受容体阻害薬は糖尿病網膜症の長期的なリスクを減らすことが示されました。
眼底検査が重要となります。
心血管の臨床研究結果を用いて、GLP-1受容体阻害薬と糖尿病網膜症の評価を行なったメタ解析のご紹介です2。
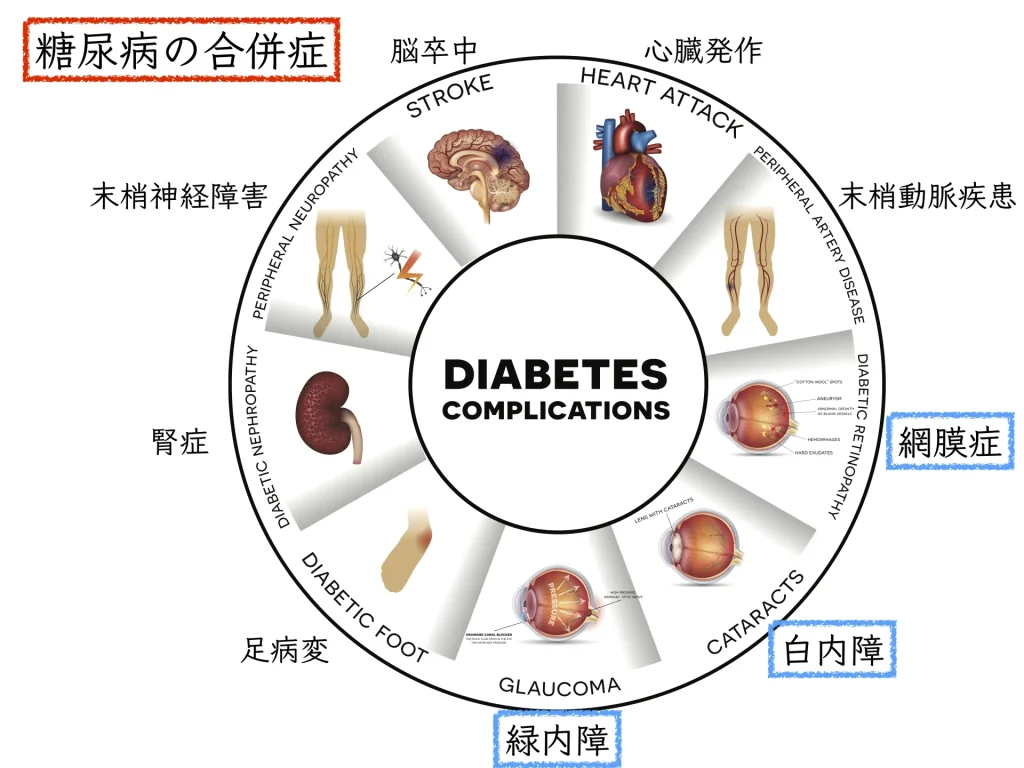
「GLP-1受容体作動薬」:糖尿病網膜症への影響(副作用)

メタアナリシス(メタ解析)とは:

メタアナリシス(meta-analysis, メタ解析)とは、研究結果を定量的かつ科学的に統合することです。
1970年代にメタアナリシスという言葉および研究の総括に対する新しいアプローチの方法が登場しました。
その後メタアナリシスは多くの科学分野で革命的な効果を発揮し、エビデンスに基づいた実践を確立したり、一見矛盾した研究結果を解決するのに役立っています3。
GLP-1受容体作動薬とは

GLP-1(Glucagon-Like Peptide-1)は食事摂取に応じて腸内で産生され、血糖値の調節に重要な役割を果たしています。

GLP-1受容体作動薬(GLP-1 RA)は「Glucagon-Like Peptide-1 Receptor Agonist」の略称で、2型糖尿病の治療に使用される薬です。
これらの薬は、体内で天然に存在するホルモンであるグルカゴン様ペプチド-1(GLP-1)の作用を模倣します。
GLP-1受容体作動薬は、2型糖尿病患者を治療する薬剤です。
図に示す作用機序により、血糖値をコントロールし、血糖値の安定化に寄与します。
また体重減少効果としても重要で、2型糖尿病患者のメタボリックシンドロームの改善にも寄与することが期待されています。
また、GLP-1には抗炎症作用があるとの言及も相次いでいます4。
GLP-1受容体作動薬は「やせ薬」「肥満治療薬」「ダイエットに効く」としても知られます5。
目(網膜)への影響も鑑み、医師の指示に基づいて正確に使用することが重要です。
GLP-1受容体作動薬:糖尿病の他、痩せ薬・肥満治療薬としても有効である理由

インスリン分泌の増加
GLP-1受容体作動薬は膵臓を刺激し、血糖値の上昇に応じてインスリンの分泌量を増やします。インスリンは、細胞がグルコースをより効率的に取り込むことで血糖値を下げる働きをします。
グルカゴン放出の減少
GLP-1受容体作動薬は、血糖値を上昇させるホルモンであるグルカゴンの放出も抑制します。これにより、肝臓から血液中に放出されるブドウ糖の量が減少します。
胃排出の遅延
GLP-1受容体作動薬は、胃の空腹感を長引かせるため、食後の血糖値の上昇を調整するのに役立ちます。
食欲抑制と体重減少
GLP-1受容体作動薬には、食欲を抑え体重減少を促進するものもあります。
GLP-1受容体作動薬は、注射剤や経口剤(飲み薬)などさまざまな製剤があります。
通常、2型糖尿病患者、特に他の経口抗糖尿病薬や生活習慣の改善だけでは十分な血糖コントロールが得られない患者さんに処方されます。
以上の作用があるため、
GLP-1受容体作動薬は、肥満治療薬としてFDAに認可されています。
(* FDA; Food and Drug Administration, アメリカ食品医薬品局)
GLP-1受容体作動薬:心血管系の影響を解析した“CVOT”
GLP-1受容体作動薬の心血管系の影響については、いくつもの臨床研究が行われました。
1.3年〜5.4年の間で、試験が終了しています。
LEADER (2016)6 N=9,340
(Liraglutide Effect and Action in Diabetes: Evaluation of Cardiovascular Outcome Results),
リラグルチド(ビクトーザ・サクセンダ)
SUSTAIN-6 (2016)7 N=3,297
(Evaluate Cardiovascular and Other Long-term Outcomes with Semaglutide in Subjects with Type 2 Diabetes),
セマグルチド(ウゴービ・オゼンピック・リベルサス)
EXSCEL (2017)8 N=14,752
(Exenatide Study of Cardiovascular Event Lowering),
エキセナチド(バイエッタ・ビデュリオンBCise)
HARMONY (2018)9 N=9,463
(Effect of Albiglutide, When Added to Standard Blood Glucose Lowering Therapies, on Major Cardiovascular Events in Subjects With Type 2 Diabetes Mellitus)
アルビグルチド(Eperzan/Tanzeum)
REWIND (2019)10 N=9,901
(Researching Cardiovascular Events with a Weekly Incretin in Diabetes; duraglutide)
デュラグルチド(トルリシティ)
PIONEER-6 (2019)11 N=3,183
(Cardiovascular Safety of Oral Semaglutide in Subjects With Type 2 Diabetes)
セマグルチド(ウゴービ・オゼンピック・リベルサス)
GLP-1 受容体作動薬は血圧を下げる効果があり、心血管系の危険因子を改善することにより、
心不全、心血管死、非致死的脳卒中、心不全による入院、全死因(あらゆる原因による)死亡率、および広範な複合腎転帰のリスクを減らし、心血管系に有益な影響をもたらすことが示されています。
長期的な影響を評価する必要はあるものの、
様々なGLP-1阻害薬に対して、心血管系の安全性が確認されています。
糖尿病網膜症に関して:
HARMONY, REWIND, PIONEER-6
では糖尿病網膜症の有病率が示されているものの、詳細に解析したものではありません。
チルゼパチド(マンジャロ)の心血管系に及ぼす影響は、現在臨床試験の途中です。
2024年10月に終了予定です。
糖尿病網膜症を発症・進行させる危険因子/「早期悪化」とは
-1024x768.webp)
糖尿病網膜症は、眼の血管系に影響を及ぼす一般的な糖尿病合併症であり、糖尿病患者の約3分の1が罹患しています。
視力低下の主な原因です。
糖尿病の進行・発症の原因には、
・糖尿病罹患期間の長さ、
・血糖値のコントロール不良、
・高血圧のコントロール不良など、
多くの危険因子が関連しています。
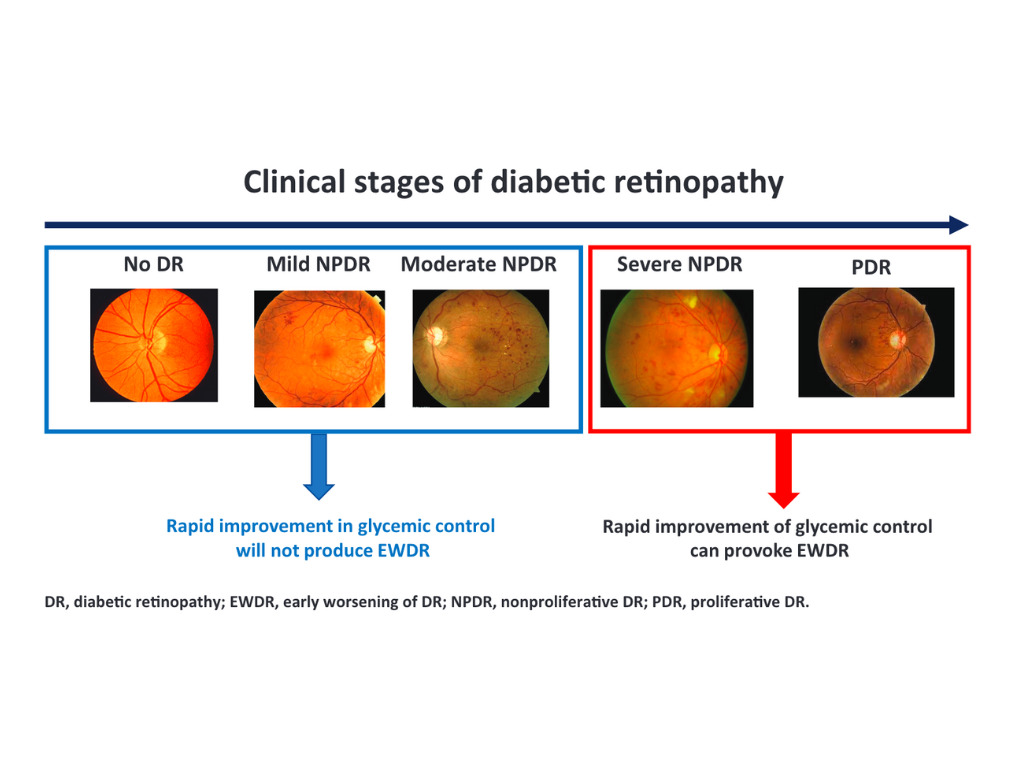
血糖値を正常に近づけることは、長期的な糖尿病網膜症のリスクを減少させます12。
でもインスリンや経口血糖降下剤(内服)を用いて糖質制限を強化すると、既存の網膜症が一過性に悪化することが古くから知られています。
厳格な糖尿病治療を開始した時点で糖尿病網膜症が悪化することを「早期悪化」と呼んでいます。
ここでいう “早期 “とは、
良好な血糖コントロールが確立されていることであり、
糖尿病罹患期間が短いことではありません13。

この研究2により、GLP-1 受容体作動薬が2型糖尿病患者の網膜症リスクを低減することが明らかにされました。
また、これまでの研究では、網膜症の状態は一時的に悪化する可能性があるものの、集中的な血糖管理による改善は3年から5年以上かかることが明らかにされています。
しかしながら、GLP-1 受容体作動薬が短期的な網膜症の悪化を示唆するエビデンスは見つかりませんでした。
(GLP-1 受容体作動薬を含む)糖尿病治療により、
厳格な血糖コントロールは、糖尿病網膜症を一時的に悪化させる可能性はあると考えられます。
でも長期的には、最終的な治療成績の改善につながります。
最新のメタ解析による見解1と併せ、
「糖尿病網膜症が一旦悪化したとしても、血糖降下する治療は長期的に重要」
と考えられます。
参考文献
- Kapoor, I., Sarvepalli, S.M., D’Alessio, D., Grewal, D.S., Hadziahmetovic, M., 2023. GLP-1 receptor agonists and diabetic retinopathy: A meta-analysis of randomized clinical trials. Survey of Ophthalmology 68, 1071–1083. https://doi.org/10.1016/j.survophthal.2023.07.002
- Bethel, M.A., Diaz, R., Castellana, N., Bhattacharya, I., Gerstein, H.C., Lakshmanan, M.C., 2021. HbA1c Change and Diabetic Retinopathy During GLP-1 Receptor Agonist Cardiovascular Outcome Trials: A Meta-analysis and Meta-regression. Diabetes Care 44, 290–296. https://doi.org/10.2337/dc20-1815
- Gurevitch, J., Koricheva, J., Nakagawa, S., Stewart, G., 2018. Meta-analysis and the science of research synthesis. Nature 555, 175–182. https://doi.org/10.1038/nature25753
- Mehdi, S.F., Pusapati, S., Anwar, M.S., Lohana, D., Kumar, P., Nandula, S.A., Nawaz, F.K., Tracey, K., Yang, H., LeRoith, D., Brownstein, M.J., Roth, J., 2023. Glucagon-like peptide-1: a multi-faceted anti-inflammatory agent. Frontiers in Immunology 14.
- Cena, H., Chiovato, L., Nappi, R.E., 2020. Obesity, Polycystic Ovary Syndrome, and Infertility: A New Avenue for GLP-1 Receptor Agonists. The Journal of Clinical Endocrinology & Metabolism 105, e2695–e2709. https://doi.org/10.1210/clinem/dgaa285
- Marso, S.P., Daniels, G.H., Brown-Frandsen, K., Kristensen, P., Mann, J.F.E., Nauck, M.A., Nissen, S.E., Pocock, S., Poulter, N.R., Ravn, L.S., Steinberg, W.M., Stockner, M., Zinman, B., Bergenstal, R.M., Buse, J.B., 2016. Liraglutide and Cardiovascular Outcomes in Type 2 Diabetes. New England Journal of Medicine 375, 311–322. https://doi.org/10.1056/NEJMoa1603827
- Marso, S.P., Bain, S.C., Consoli, A., Eliaschewitz, F.G., Jódar, E., Leiter, L.A., Lingvay, I., Rosenstock, J., Seufert, J., Warren, M.L., Woo, V., Hansen, O., Holst, A.G., Pettersson, J., Vilsbøll, T., 2016. Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes. New England Journal of Medicine 375, 1834–1844. https://doi.org/10.1056/NEJMoa1607141
- Holman, R.R., Bethel, M.A., Mentz, R.J., Thompson, V.P., Lokhnygina, Y., Buse, J.B., Chan, J.C., Choi, J., Gustavson, S.M., Iqbal, N., Maggioni, A.P., Marso, S.P., Öhman, P., Pagidipati, N.J., Poulter, N., Ramachandran, A., Zinman, B., Hernandez, A.F., 2017. Effects of Once-Weekly Exenatide on Cardiovascular Outcomes in Type 2 Diabetes. New England Journal of Medicine 377, 1228–1239. https://doi.org/10.1056/NEJMoa1612917
- Hernandez, A.F., Green, J.B., Janmohamed, S., et al., 2018. Albiglutide and cardiovascular outcomes in patients with type 2 diabetes and cardiovascular disease (Harmony Outcomes): a double-blind, randomised placebo-controlled trial. The Lancet 392, 1519–1529. https://doi.org/10.1016/S0140-6736(18)32261-X
- Gerstein, H.C., Colhoun, H.M., Dagenais, G.R., et al, 2019. Dulaglutide and cardiovascular outcomes in type 2 diabetes (REWIND): a double-blind, randomised placebo-controlled trial. The Lancet 394, 121–130. https://doi.org/10.1016/S0140-6736(19)31149-3
- Husain, M., Birkenfeld, A.L., Donsmark, M., Dungan, K., Eliaschewitz, F.G., Franco, D.R., Jeppesen, O.K., Lingvay, I., Mosenzon, O., Pedersen, S.D., Tack, C.J., Thomsen, M., Vilsbøll, T., Warren, M.L., Bain, S.C., 2019. Oral Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes. New England Journal of Medicine 381, 841–851. https://doi.org/10.1056/NEJMoa1901118
- Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33), 1998. . The Lancet 352, 837–853. https://doi.org/10.1016/S0140-6736(98)07019-6
- Simó, R., Franch-Nadal, J., Vlacho, B., Real, J., Amado, E., Flores, J., Mata-Cases, M., Ortega, E., Rigla, M., Vallés, J.-A., Hernández, C., Mauricio, D., 2023. Rapid Reduction of HbA1c and Early Worsening of Diabetic Retinopathy: A Real-world Population-Based Study in Subjects With Type 2 Diabetes. Diabetes Care 46, 1633–1639. https://doi.org/10.2337/dc22-2521
![たける眼科 | 福岡市早良区 高取商店街[西新駅/藤崎駅]](https://takeru-eye.com/wp-content/uploads/2022/10/takeru_logo_for-WP-header.png)